В САЩ одобриха първия биоподобен лекарствен продукт за лечение на множествена склероза
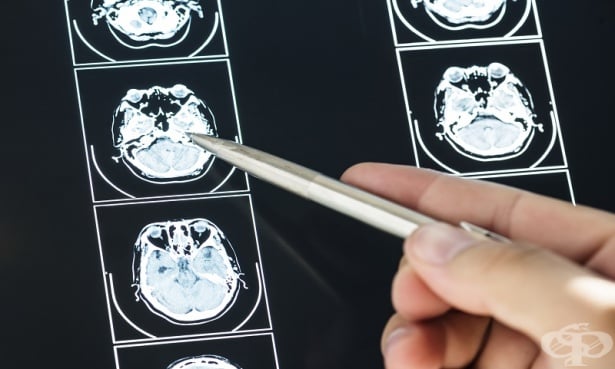
Агенцията за контрол на храните и лекарствата на САЩ (FDA) одобри първия биоподобен лекарствен продукт за лечение на пациенти, диагностицирани с рецидивиращи форми на множествена склероза.
|
Биоподобните лекарствени продукти са медикаменти, които са много сходни с вече одобрени референтни биофармацевтични лекарства. Те се предлагат на много по-ниски цени, което увеличава достъпа до лечение на множество хора, които живеят с редица тежки заболявания. |
Одобреният медикамент Natalizumab-sztn представлява продукт за интравенозно приложение, биоподобен на натализумаб – селективен имуносупресор, който преустановява преминаването на агранулоцити в паренхимната тъкан, като по този начин намалява възпалителния процес в централната нервна система при пациенти с множествена склероза.
>>> Вирусът на Епщайн-Бар може да предизвика множествена склероза
„Биоподобните лекарства предлагат допълнителни ефективни възможности за лечение, които имат потенциала да увеличат достъпа на хора, живеещи с рецидивиращи форми на множествена склероза.“, коментира д-р Пол Лий от Центъра за оценка и изследване на лекарства на FDA. „Одобрението може да има значително въздействие върху управлението на тежкото заболяване, което оказва голямо въздействие върху социалното и икономическото благополучие на пациентите и техните семейства.“
Одобрение и рискове
Одобрението на Natalizumab-sztn се основава на данни, които не показват клинично значими разлики в безопасността и ефективността между биоподобния и референтния натализумаб. Сходният продукт е одобрен за лечение на пациенти с рецидивиращи форми на множествена склероза – пристъпно-ремитентна и вторично прогресираща.
И при двата медикамента има предупреждение за повишен риск от прогресивна мултифокална левкоенцефалопатия (ПМЛ) – инфекциозно прогресиращо заболяване на централната нервна система, което може да доведе до тежко увреждане или смърт. Рисковите фактори за ПМЛ включват наличие на антитела срещу JC вируса, по-продължителна терапия и предишна употреба на имуносупресори.
„Тези фактори трябва да се разглеждат в контекста на очакваните ползи при започване и продължаване на лечението, като е необходимо лекарите да наблюдават пациентите и да прекратят приема незабавно при първия признак или симптом, предполагащ прогресивна мултифокална левкоенцефалопатия.“, предупреждават от FDA.
Рисковете от прогресивна мултифокална левкоенцефалопатия означава, че биоподобният медикамент ще бъде достъпен само чрез програма за разпространение на лекарства с ограничен достъп, съгласно стратегия за оценка и смекчаване на риска (REMS). Програмата изисква лекарите, предписващи натализумаб, и аптеките, предлагащи медикамента, да са сертифицирани, а пациентите да са включени в REMS. Предписващите трябва да оценят пациентите за период от 3 до 6 месеца след първата инфузия и на всеки 6 месеца след това, както и при спиране на лечението и половин година по-късно.
Допълнителните предупреждения включват рискове от херпесни инфекции, тромбоцитопения, имуносупресия или сериозни реакции на свръхчувствителност, включително анафилаксия и хепатотоксичност, отбелязват от FDA. Най-честите нежелани реакции, свързани с натализумаб, са главоболие и умора. Освен това могат да се развият артралгия, инфекция на пикочните пътища, инфекция на долните дихателни пътища, гастроентерит, вагинит, депресия, болка в крайниците, стомашен дискомфорт, диария и обрив.
Увеличаване на достъпа до лечение
Националното дружество за множествена склероза наскоро публикува позиция относно биоподобните лекарствени продукти, отбелязвайки, че появата им на пазара може да доведе до увеличаване на достъпа до ефективни лечения, да подобри управлението на болестта и да помогне за ограничаване на разходите за здравеопазване. Дружеството също очертава ролите, които да поемат пациентите и лекарите, когато към лечението на множествената склероза се включват биоподобни медикаменти.
First Multiple Sclerosis Biosimilar Approved: https://www.medpagetoday.com/neurology/multiplesclerosis/106045
Продукти свързани с НОВИНАТА
ЕНТЕРОСАН МС таблетки * 60
ТермолабилниНОВИНАТА е свързана към
- Множествена склероза
- Лечение с баклофен
- Разработват терапия за множествена склероза, която може да спре прогресията на болестта
- Евокирани (предизвикани) потенциали
- Методи за диагностициране на случаи на множествена склероза от 1978г.
- Лечение на множествена склероза
- Проф. Пенко Шотеков и д-р Детелина Стоилова с нови книги за множествената склероза
- Таня Бейрийска – жената, която победи нелечимото заболяване Множествена склероза с метод, базиран на кетонната диета
- Изследвания за множествена склероза с отличието Оскар за наука
- Бързи темпове на разрастване за "Тева" до 1989г.


Коментари към В САЩ одобриха първия биоподобен лекарствен продукт за лечение на множествена склероза