Сърдечна саркоидоза
Саркоидозата представлява мултисистемна грануломатозна болест с неизвестна етиология, която се характеризира с наличие на неказеинифициращи грануломи в засегнатите органи. В началото се установяват едно или повече от следните нарушения: двустранна хилусна аденопатия, ретикулерни сенки, лезии на кожата и/или очите. При половината от засегнатите болестта се открива случайно при рентгенография преди да се е изявило клинично. При над 90% от случаите са засегнати белите дробове. При засягане на сърцето може да се увреди всяка една част – проводна система, миокард, клапи, перикард. Сърдечната саркоидоза може да бъде доброкачествена, случайно открита форма на болестта, или животозастрашаващо състояние. Клинични данни за миокардно засягане се откриват едва при 5% от пациентите със саркоидоза, но на аутопсия се открива субклинично засягане при 20-30% от случаите1.
Клинични изяви
Зависят от локализацията и степента на грануломатозно възпаление. Тъй като най-често се засяга белият дроб, обичайни симптоми са кашлица, задух и гръдна болка. Други прояви са умора, отпадналост, фебрилитет и загуба на тегло. Повече от 30% имат екстраторакални прояви2. Сърдечното засягане може да предшества, следва или да се появи заедно със засягане на белите дробове и други органи. Най-често се изразява под форма на ритъмни и проводни нарушения и се дължи на саркоидни грануломи, които стават фокус на патологичен автоматизъм или риентри механизъм. Проводните нарушения са по типа на АV блок от различен тип1 и могат да бъдат тихи или да прогресират до пълен блок и до синкоп3. При 22% от пациентите със саркоидоза се откриват продължителни и непродължителни камерни тахикардии, камерни екстрасистоли4. Камерните тахикардии или AV блок са причина за внезапна сърдечна смърт и летален изход при 25% до 65% от болните със сърдечна саркоидоза5.
При масивна инфилтрация на миокарда с грануломи се развива сърдечна недостатъчност с увреждане на систолната и диастолната функция. Има случаи на пациенти с левокамерна аневризма, с предположението, че тя може да се дължи на терапия с кортикостероиди, които превръщат грануломите в цикатрициална тъкан6. Диагнозата сърдечна саркоидоза при наличие на кардиомегалия и сърдечна недостатъчност може да бъде трудна, особено при пациенти без засягане на други органи. На някои от тях се поставя диагноза идиопатична дилатативна кардиомиопатия. Пациентите със саркоидоза имат по-често високостепенен AV блок, патологично изтъняване на стената, нарушения в кинетиката на стените, перфузионни дефекти, засягащи антеросепталните и апикалните региони.
Надкамерните аритмии са редки и са под форма на пароксизмална надкамерна тахикардия, предсърдно трептене и мъждене2. Клапните нарушения се представят с митрална инсуфициенция, която се дължи на засягане на папиларен мускул от саркоиден гранулом и обикновено е преходна и рядко налага клапно протезиране поради хемодинамична нестабилност. Рядко се засяга аортната клапа и корен с развитие на аортна регургитация и аневризма.
Сърдечното засягане при саркоидоза може да доведе до симптоми и ЕКГ-находки, които могат да симулират миокарден инфаркт7. Засягането на перикарда е рядко8. Белодробно сърце може да се развие в резултат на масивна белодробна фиброза. При някои пациенти след овладяване на процеса с кортикостероиди се наблюдава регресия на деснокамерната хипертрофия.
Диагностични тестове
Няма специфични тестове за диагностициране на сърдечна саркоидоза. Повечето са с ниска специфичност или сензитивност и не е позната оптимална диагностична стратегия9. При пациенти с установена белодробна саркоидоза клиницистите трябва активно да търсят белези на засягане на сърцето. Сърдечна саркоидоза се диагностицира по-често при симптомни пациенти, които са с много по-висок риск от безсимптомните10.
Ендомиокардна биопсия
Тя е доказан тест за установяване на сърдечно засягане от саркоидоза. Може обаче тестът да е фалшиво негативан поради нехомогенно засягане на миокарда. Миокардните саркоидни грануломи са с тенденция да бъдат разположени базално, докато биопсията обикновено се прави на апикалния септум, така че процедурата се оказва с ниска сензитивност, доближавайки 20% при една серия от 26 пациента11. Независимо от това, ранната ендомиокардна биопсия се препоръчва при обсъждане на сърдечна саркоидоза. Негативната биопсия обаче не изключва диагнозата.
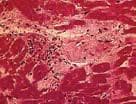
Фигура 1. Грануломатозно възпаление в миокарда (Courtesy of Om P Sharma, MD).
Рентгенография
С нея може да се открие лека до умерена кардиомегалия, застойна сърдечна недостатъчност, перикарден излив или левокамерна аневризма и находки на белодробна саркоидоза.
Електрокардиография
Близо 70% от пациентите със саркоидоза имат нарушения в ЕКГ1.
Холтер-мониториране
С него може да се документират находки, които липсват на ЕКГ в покой12. Препоръчва се провеждането на Холтер ЕКГ и тест с натоварване като рутинни при подозиране на сърдечна саркоидоза.
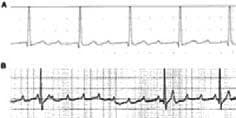
Фигура 2. ЕКГ в покой с АV-бл I степен (А); ЕКГ при натоварване с пълен AV-блок (В) (по Langer W, Iversen E, Vestbo J, Viskum K. 1995).
Ехокардиография
С нея може да се документират последици от саркоидоза, като левокамерна аневризма и дилатация, клапни увреждания, нарушения в кинетиката, но не може да индентифицират грануломи и да се отхвърли или докаже саркоидоза. Миокардът, в частност междукамерният септум или свободната стена на лява камера, изглеждат хиперехогенни при грануломатозно засягане и формиране на цикатрициална тъкан13.
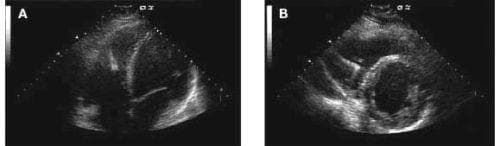
Фигура 3. Ехокардиография на пациент 4 години и 9 месеца след изява на сърдечната саркоидоза: (A) апикална 4-кухинна позиция и (B) парастерналната по-къса ос показват дилатация на дясна камера и хипокинезия на септум (Nat Clin Pract Cardiovasc Med 2008).
Радионуклеидни методи
Сцинтиграфия с талий-201 може да е полезна за подсказване на миокардно засягане и за изключване на сърдечна дисфункция, която се дължи на коронарна болест. При тест с натоварване може да се имитира коронарна боласт, но при саркоидоза перфузионните дефекти намаляват по размер по време на натоварването15. Прогресията или регресията на талиевите перфузионни дефекти е полезно за мониториране на отговора на лечение16. Може да се използва и комбинация от талий-201 и галий-67 (който се натрупва в зоните на активно възпаление)17. Позитрон-емисионната томография (РЕТ) може да установи рано възпаление при сърдечна саркоидоза и развитие на напреднала фиброза18. Радионуклеидните методи не се препоръчват рутинно за скрининг при пациенти с други органни засягания поради неспецифичните резултати19.
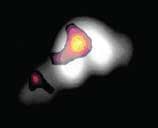
Фигура 4. SPECT изображение в покой, използващо 99mTc-Hexamibi и 111In-pentetreotide, което показва съчетание на апикален перфузионен дефект, установен с 99mTc-Hexamibi и натрупване на 111In-pentetreotide на същото място.
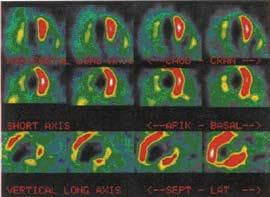
Фигура 5. SPECT сцинтиграфия с tallium-201 установява дефекти в натрупването в областта на септум, връх, долна стена на лява камера (по R. Zimmermann, A. Haunstetter, W. Kuebler).
Ядрено-магнитен резонанс (ЯМР)
Използването му не е подкрепено с достатъчно опит. Използването на гадолиний-DTPA позволява установяване на сърдечно засягане и оценяване на ефикасността на стероидната терапия9.
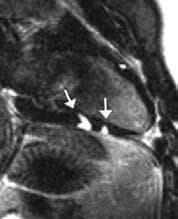
Фигура 6. ЯМР, усилен с Gd-DTPA, покзва грануломи с фиброза и образуване на цикатрикс (по Smedema JP, Snoep G, van Kroonenburgh MP, et al. 2005).
Коронарна ангиография
Полезнае за изключване на атеросклеротична коронарна болест. Може да има дефекти в пълненето на съдовете в резултат на грануломи в миокарда.
Електрофизиологично изследване
Прави се за оценка на ритъмната патология и преценка на индикациите за имплантиране на кардиовертер-дефибрилатор (ICD).
Прогноза при симптоматична сърдечна саркоидоза. Не е добре определена. При серия аутопсии на 113 пациента се прави заключение, че продължителността на живот при повечето е около две години след развитие на сърдечни симптоми и белези. В две големи проучвания са установени следните резултати: 44% преживяват повече от пет години след поставянето на диагноза и 75% от пациентите на стероидна терапия преживяват пет години5. Повечето умират от усложнения на саркоидозата като камерни тахиаритмии, нарушения в провеждането и прогресивна кардиомиопатия6.
Лечениe на сърдечна саркоидоза
Насочено е към контролиране на възпалението и фиброзата, които характеризират болестта, и съхраняване на сърдечната функция и структура. За кортикостероидите се твърди, че забавят прогресията на възпалението и фиброзата чрез способността си да потискат възпалителния отговор. В ретроспективно проучване, базирано на преживяемост, при 104 случая на сърдечна саркоидоза преживяемостта при лекувани с кортикостероиди е по-добра (64% срещу 40% при нелекувани)20. Много е важно ранното започване на лечение5. Ефектът на стероидите върху камерните аритмии не е много сигурен и някои автори препоръчват прилагане на имплантируем кардиовертер дефибрилатор (ICD)21. Не е известна оптимална доза на кортикостероиди и изборът се определя от баланса на рисковете от странични ефекти и ползата22. Необходими са начални дози от 60 до 80 mg prednisone дневно. Дозата може да се редуцира на поддържащи нива от 10 до 15 mg/дневно за период от шест месеца. Рецидивите са чести след спиране на стероидната терапия и тогава отново трябва да се започне лечение или да се повиши дозата. Други алтернативни медикаменти при пациенти, които не отговарят на кортикостероиди, са chloroquine, hydroxychloroquine, cyclosporine и methotrexate. Пейсмейкър и/или ICD се прилагат при камерни тахиаритмии или нарушения в проводимостта6.
Хирургия и трансплантация
Хирургично лечение може да е необходимо за корекция на митрална клапна болест или резекция на камерна аневризма. Сърдечната трансплантация се прилага при млади пациенти с тежка и необратима сърдечна недостатъчност, но са възможни рецидиви на болестта23.
Лилия Демиревска, Ивайло Даскалов, Александър Александров, Станислав Иванов, Добромир Гочев
д-р Лилия Демиревска, Клиника по кардиология и ревматология, Военномедицинска академия – София
д-р Ивайло Даскалов, Клиника по кардиология и ревматология, Военномедицинска академия – София
д-р Александър Александров, Клиника по кардиология и ревматология, Военномедицинска академия – София
д-р Станислав Иванов, Клиника по кардиология и ревматология, Военномедицинска академия – София
доц. д-р Добромир Гочев, д.м., Клиника по кардиология и ревматология, Военномедицинска академия – София
Литература
1.Chapelon-Abric C, de Zuttere D, Duhaut P, et al. Cardiac Sarcoidosis: A Retrospective Study of 41 Cases. Medicine (Baltimore) 2004; 83:315.
2.Ahmad K, Kim YH, Spitzer AR, et al. Total nodal radiation in progressive sarcoidosis. Case report. Am J Clin Oncol 1992; 15: 311
3.Yoshida Y, Morimoto S, Hiramitsu S, et al. Incidence of cardiac sarcoidosis in Japanese patients with high-degree atrioventricular block. Am Heart J 1997; 134: 382
4.Sekiguchi M, Numao Y, Imai M. Clinical and histological profile of sarcoidosis for the heart and acute idiopathic myocarditis. Concepts through a study employing myocardial biopsy. Jpn Circ J 1980; 44: 249
5.Yazaki Y, Isobe M, Hiroe M, et al. Prognostic determinants of long-term survival in Japanese patients with cardiac sarcoidosis treated with prednisone. Am J Cardiol 2001; 88: 1006
6.Roberts WC, McAllister HA, Ferrans VJ. Sarcoidosis of the heart. A clinicopathologic study of 35 necropsy patients (group 1) and review of 78 previously described necropsy patients (group 11). Am J Med 1977; 63: 86
7.Wait J, Movahed A. Anginal chest pain in sarcoidosis. Thorax 1989; 44: 391
8.Navaneethan SD, Venkatesh S, Shrivastava R, et al. Recurrent pleural and pericardial effusions due to sarcoidosis. PLoS Med 2005; 2: e63
9.Smedema JP, Snoep G, van Kroonenburgh MP, et al. Evaluation of the accuracy of gadolinium-enhanced cardiovascular magnetic resonance in the diagnosis of cardiac sarcoidosis. J Am Coll Cardiol 2005; 45: 1683
10.Smedema JP, Snoep G, van Kroonenburgh MP, et al. Cardiac involvement in patients with pulmonary sarcoidosis assessed at two university medical centers in the Netherlands. Chest 2005; 128: 30
11.Uemura A, Morimoto S, Hiramitsu S, et al. Histologic diagnostic rate of cardiac sarcoidosis: Evaluation of endomyocardial biopsies. Am Heart J 1999; 138: 299
12.Langer W, Iversen E, Vestbo J, Viskum K. Electrocardiographic changes in patients with intrathoracic sarcoidosis: Influence on prognosis. Sarcoidosis 1995; 12: 42
13.Fahy J, Marwick T, McGreery C, Quigley R, et al. Doppler echocardiography detection in patients with pulmonary sarcoidosis. Chest 1996; 109: 62
14.Haywood LJ, Sharma OP, Siegel ME. Detection of myocardial sarcoidosis by thallium-201 imaging. J Natl Med Assoc 1982; 74: 959
15.Roberts SD, Mirowski GW, Wilkes D, et al. Sarcoidosis. Part II: extrapulmonary and systemic manifestations. J Am Acad Dermatol 2004; 51: 628
16.Mana J. Nuclear Imaging: 67-gallium, 201-thallium, 18F-labeled Fluoro-2-deoxy-D-glucose positron emission tomography. Clin Chest Med 1997; 18: 799
17.Okayama K, Kurata C, Tawarahara K, et al. Diagnostic and prognostic value of myocardial scintigraphy with thallium-201 and gallium-67 in cardiac sarcoidosis. Chest 1995; 107: 330
18.Okumura W, Iwasaki T, Toyama T, et al. Usefulness of fasting 18F-FDG PET in identification of cardiac sarcoidosis. J Nucl Med 2004; 45: 1989
19.Sharma OP, Maheshwari A, Thaker K. Myocardial sarcoidosis. Chest 1993; 103: 253
20.Takada K, Ina Y, Yamamoto M, et al. Prognosis after pacemaker implantation in cardiac sarcoidosis in Japan. Clinical evaluation of corticosteroid therapy. Sarcoidosis 1994; 11: 113
21.Belhassen B, Pines A, Laniado S. Failure of corticosteroid therapy to prevent induction of ventricular tachycardia in sarcoidosis. Chest 1989; 95: 918
22.du Bois RM. Corticosteroids in sarcoidosis: Friend or foe? Eur Respir J 1994; 7: 1203
23.Valantine HA, Tazelaar HD, Macoviak J, et al. Cardiac sarcoidosis: response to steroids and transplantation. J Heart Transplant 1987; 6: 244
Коментари към Сърдечна саркоидоза