Експертите на FDA разрешиха за спешна употреба бустерна доза от ваксината срещу COVID-19 на „Moderna”
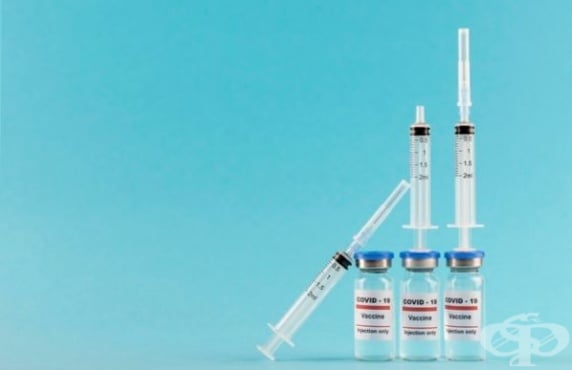
Съветниците по ваксините към Агенцията за контрол на храните и лекарствата на САЩ (FDA) приеха вчера, 14 октомври, единодушно препоръка за разрешаване за спешна употреба на бустерната доза на ваксината срещу COVID-19 на фармацевтичната компания „Moderna”.
Консултативният комитет за ваксините и свързаните с тях биологични продукти на FDA се съгласи, че използването на трета доза ще бъде безопасно и ефективно при някои хора шест месеца след завършване на ваксинационния цикъл.
„Moderna” поиска разрешение за спешна употреба за половин доза от ваксината, която да се използва като бустер за определени групи хора.
Препоръка за разрешение на бустерна доза на ваксината на „Moderna”
Всичките 19 членове на Комитета подкрепиха разрешаването на бустерна доза от 50 микрограма – половината от стандартната доза от 100 микрограма. Тя ще се прилага най-малко шест месеца след втората доза и само на определени групи – възрастни на 65 и повече години, хора на възраст от 18 до 64 години, които са изложени на висок риск от тежък COVID-19, и лица, чиято работа е свързана с риск от усложнения или тежко протичане на заболяването.
Искането на „Moderna” включва групите, за които е разрешена трета доза от иРНК ваксината на „Pfizer“. Бустер от ваксините срещу COVID-19 на „Moderna“ и „Pfizer“ вече се прилагат на имунокомпрометирани лица.
Срещата на Консултативният комитет за ваксините и свързаните с тях биологични продукти ще продължи и днес, 15 октомври, когато се очаква членовете да гласуват бустерна доза на ваксината на „Johnson & Johnson“ и ще разгледат презентация за смесването на ваксини.
Комитетът на независимите съветници на FDA обикновено обсъжда и прави препоръки относно разрешенията и одобренията на ваксините, а след това агенцията взима окончателното решение.
Консултативният комитет за имунизационните практики на Центровете за контрол и превенция на заболяванията (CDC) планира да обсъди бустерните дози на 21 октомври.
Експертите са разединени относно необходимостта от трета доза и прилагането й на лица под 18 години
Въпреки единодушното гласуване членовете на Консултативния комитет не са напълно убедени, че данните показват, че е необходима бустерна доза или че тя увеличава защитата.
„Данните не са перфектни, но това са извънредни времена и трябва да работим с наличната информация.“, казва д-р Ерик Рубин, главен редактор на списанието „New England Journal of Medicine“ и професор в Харвардското училище по обществено здраве "Т. Х. Чан".
“Не можем да си позволим заразени или болни здравни работници, тъй като в някои части на страната има сериозен недостиг на персонал.“, казва д-р Стенли Перлман, професор по педиатрия в Калифорнийския университет в Сан Диего.
След гласуването вчера членовете бяха помолени да обмислят разширяване обхвата на разрешението за спешна употреба, въпреки че някои от тях заявиха, че не подкрепят широкото използване на бустери.
„Изобщо не съм съгласен да се прилага трета доза на лица под 18-годишна възраст.“, казва Пол Офит, директор на Центъра за ваксини и професор по педиатрия в Детската болница във Филаделфия. „Впечатлен съм от факта, че продължаваме да имаме отлична защита срещу умерено до тежко протичане на COVID-19 при всички възрастови групи, независимо от по-заразния вариант „Делта“. И просто мисля, че продължаваме да изпращаме грешни послания, използвайки термини като пробив, което кара хората да се чувстват незащитени, в случай че не са си поставили трета доза.“, добавя той.
Д-р Майкъл Курила, директор на Отдела за клинични иновации в Националния център за насърчаване на транслационните науки към Националните здравни институти, също е съгласен, че не е необходима кампания за поставяне на бустерни дози.
Част от членовете на Консултативният комитет за ваксините и свързаните с тях биологични продукти са на мнение, че в момента най-важната задача е да се повиши нивото на ваксинация чрез насърчаване на неваксинираните лица в САЩ.
Ако FDA даде разрешение за спешна употреба на бустерната доза на „Moderna“, съветниците за ваксините към Центровете за контрол и превенция на заболяванията ще обсъдят на кои групи да се препоръча. Третата доза ще може да се прилага, след като директорът на CDC подпише препоръката за нейното поставяне.
-
 Защо FDA не препоръчва бустерна ваксина за всички граждани
Защо FDA не препоръчва бустерна ваксина за всички граждани
-
 FDA разреши поставянето на трета доза иРНК ваксина срещу COVID-19 на имунокомпрометирани лица
FDA разреши поставянето на трета доза иРНК ваксина срещу COVID-19 на имунокомпрометирани лица
-
 FDA добави предупреждение за рядко сърдечно възпаление в листовките на ваксините на „Pfizer“ и „Moderna“
FDA добави предупреждение за рядко сърдечно възпаление в листовките на ваксините на „Pfizer“ и „Moderna“
-
 FDA предупреждава за негативни ефекти след приема на ивермектин при лечение на COVID-19
FDA предупреждава за негативни ефекти след приема на ивермектин при лечение на COVID-19
НОВИНАТА е свързана към
- Кирил Петков: От януари 2022 г. всеки пенсионер, който се ваксинира срещу COVID-19, ще получи добавка от 75 лв.
- Как да разговаряте с хора, които се съмняват във ваксините срещу COVID-19
- Капки за очи, одобрени от FDA, могат да заменят очилата за четене
- Да се допускат ли до учебните заведения деца без ваксини
- Ваксината срещу коронавирус може да облекчи симптомите при дълго протичане на COVID-19
- Ваксината срещу COVID-19 на GSK и Medicago показва висока ефективност във фаза II на клиничните изпитвания
- Ваксината VLA2001 срещу COVID-19 на Valneva показва много добри резултати в третата фаза на изпитванията
- 8 септември 2021 г.: Бойкот на противоепидемичните мерки в България, броят на заразените с COVID-19 расте
- На 31 юли 2020-а НС одобри промени в Закона за лечебните заведения
- Ваксината срещу COVID-19 на „Pfizer” е безопасна за деца на възраст от 5 до 11 години
Коментари към Експертите на FDA разрешиха за спешна употреба бустерна доза от ваксината срещу COVID-19 на „Moderna”